Дифенилкетон
| Дифенилкетон | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
Дифенилкетон |
| Традиционные названия | Бензофенон |
| Хим. формула | (С6H5)2CO |
| Рац. формула | С13H10O |
| Физические свойства | |
| Молярная масса | 182,2214 г/моль |
| Плотность | 1,11 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 48,1 °C |
| • кипения | 305,4 °C |
| • вспышки | 143 °C |
| • самовоспламенения | 560 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 0.1 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1.5893 |
| Классификация | |
| Рег. номер CAS | 119-61-9 |
| PubChem | 3102 |
| Рег. номер EINECS | 204-337-6 |
| SMILES | |
| InChI | |
| ChEBI | 41308 |
| ChemSpider | 2991 |
| Безопасность | |
| Токсичность | токсичен (покраснение, боль в горле) |
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Дифенилкетон (бензофенон, дифенилметанон) — это органическое соединение, относится к классу ароматических кетонов. Обладает свойством поглощать и отражать УФ-излучение. Ингибитор полимеризации стирола, фиксатор запаха, фотостабилизатор.
Содержание
Свойства
Общие
Способен поглощать и отражать УФ-излучение, обладает некоторыми свойствами консервантов, имеет специфический запах, напоминающий запах герани и розы.
Физические свойства
Существует в двух аллотропных модификациях — лабильной и стабильной. Лабильная форма — бесцветные кристаллы; tпл.=26,5 °C; tкип.=305 °C. Стабильная форма — ромбические кристаллы. Физические свойства стабильной формы описаны в таблице.
Химические свойства
Мягкий окислитель. Химические свойства соответствуют кетонам и ароматическим соединениям. Существует одна характерная реакция для дифенилкетона. Если поместить в герметичную ампулу смесь дифенилкетона с этиловым спиртом и оставить ампулу под действием солнечного света в течение недели, то из-за свойства дифенилкетона поглощать электромагнитное излучение может произойти окислительно-восстановительная реакция, этиловый спирт при этом окисляется до этаналя и образовывается дигидрокситетрафенилэтан с выходом более 80 %.
Применение
Общее
Дифенилкетон способен поглощать и отражать УФ-излучение, благодаря чему он может длительное время сохранять вещества от действия света. Поэтому его используют в качестве фотостабилизатора и фиксатора запаха и добавляют в отдушку для мыла, некоторые духи, косметику для защиты кожи от УФ-излучения, а также в некоторые красители и пигменты для защиты от УФ-излучения. Более широко получили своё применение производные бензофенона, одним из которых является кетон Михлера, тоже фотосенсибилизатор.
Парфюмерия
Парфюмерные изделия упаковываются в прозрачные флаконы для того, чтобы создавать представительный вид, но от этого они не достаточно защищены от ультрафиолетового излучения, поэтому в парфюмерные изделия добавляют бензофенон, который дополнительно выполняет функции фиксатора запаха. Сам бензофенон хоть и имеет запах герани и розы, но не принимает активного участия в формировании запаха.
Косметика
В косметике активно используются солнцезащитные фильтры на основе бензофенона, такие как бензофенон-1, бензофенон-2, бензофенон-3 (оксибензон), бензофенон-4 и другие. Они защищают кожу от широкого спектра УФ-излучения.
Получение
Получить дифенилкетон можно несколькими способами:
Разложение бензоата кальция
Реакция бензола с тетрахлорметаном и гидроксидом натрия
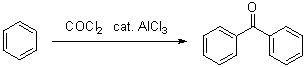
Реакция бензола с фосгеном
Открытие
Дифенилкетон был независимо получен Э. М. Пелиго и Мичерлихом в 1834.
Токсичность
В больших концентрациях бензофенон способен вызывать покраснение кожи и слизистых оболочек, при вдыхании паров отёки и боли в горле. Последние исследования показали, что бензофенон провоцирует аллергическую реакцию организма даже при небольших количествах. Следует препятствовать попаданию больших количеств бензофенона на кожу и слизистые оболочки. Токсичен при приёме внутрь.
Попадая в морскую воду с кожи купающихся людей, бензофенон-3 (оксибензон), содержащийся в кремах от загара, уничтожает личинки кораллов, препятствуя их размножению. Токсичен для них уже в концентрации 62 части на триллион частей воды, в воде у некоторых южных пляжей этот уровень превышен в 12 раз.