
Ядерные тельца
Я́дерные тельца́ (англ. nuclear bodies) — субкомпартменты внутри ядра, не окружённые мембранами, но представляющие собой отдельные, морфологически различимые комплексы белков и РНК. К числу ядерных телец относят ядрышко, тельце Кахаля и другие немембранные структуры. В основе биогенеза ядерных телец лежат одни и те же общие принципы, такие как способность к формированию de novo (с нуля), самоорганизация, а также роль РНК как структурного элемента. Контроль биогенеза ядерных телец необходим для правильного изменения архитектуры ядра в ходе клеточного цикла и лежит в основе ответа клетки на внутри- и внеклеточные стимулы. Многие ядерные тельца осуществляют специфические функции — например, синтез и процессинг пре-рибосомных РНК в ядрышке, накопление и сборку компонентов сплайсосом в ядерных спеклах или накопление молекул РНК в параспеклах. Механизмы, которые обеспечивают выполнение ядерными тельцами этих функций, очень разнообразны. В некоторых случаях ядерное тельце может служить местом протекания определённых процессов, например, транскрипции. В других случаях ядерные тельца, по-видимому, опосредованно регулируют локальные концентрации своих компонентов в нуклеоплазме. Хотя большинство ядерных телец имеет сферическую форму, большинство из них можно идентифицировать по уникальной морфологии, которая выявляется при помощи электронной микроскопии, и по расположению в ядре. Подобно цитоплазматическим органеллам, ядерные тельца содержат специфический набор белков, которые определяют их структуру на молекулярном уровне.
Содержание
Физические свойства
Многие ядерные тельца ведут себя подобно капле вязкой жидкости. Например, в ооцитах лягушки Xenopus ядрышки имеют почти идеально сферическую форму. Когда два ядрышка встречаются, они сливаются друг с другом, образуя ядрышко большего размера. Подобное слияние описано для телец Кахаля, телец гистоновых локусов, ядерных спеклов и других телец. Однако некоторые ядерные тельца, например, ядрышко, состоят из нескольких структурных компонентов, о чём свидетельствуют данные электронной микроскопии. На первый взгляд, это противоречит представлению о ядерных тельцах как о каплях вязкой жидкости. В ооцитах Xenopus и гранулярный компонент, и плотный фибриллярный компонент ядрышек могут подвергаться слиянию и обмениваться белками, но гранулярный компонент делает это быстрее. Ключевые белки гранулярного и плотного фибриллярного компонентов — нуклеофозмин и фибрилларин соответственно — в очищенном виде могут формировать капли в присутствии РНК, однако капли нуклеофозмина сливаются и обмениваются белками быстрее, чем белки фибрилларина. Физически капли нуклеофозмина представляют собой вязкую жидкость, а капли фибрилларина вязкоупруги, что и объясняет их замедленную динамику. Когда очищенные нуклеофозмин и фибрилларин объединяют в одну каплю, они образуют несмешивающиеся фазы, похожие на ядрышки: маленькие капельки фибрилларина находятся внутри более крупных капель нуклеофозмина. Несмешиваемость фаз обеспечивается разностью в поверхностном натяжении, так как капли фибрилларина в водном растворе более гидрофобны, чем капли нуклеофозмина. Возможно, похожим образом объясняется неспособность разных ядерных телец сливаться друг с другом. Например, ядрышки и тельца Кахаля нередко находятся в близком контакте, но никогда не сливаются, возможно, из-за высокого межфазного энергетического барьера.
Динамика
Общим свойством всех ядерных телец является их структурная стабильность. Отдельные ядерные тельца различимы на протяжении интерфазы — от начала G1-фазы до выхода из G2-фазы. В течение интерфазы ядерные тельца подвергаются динамическим перемещениям внутри ядра, причём чем крупнее тельце, тем меньше оно перемещается. Крупные тельца, такие как ядрышки и спеклы, достигающие 2—3 мкм в диаметре, практически неподвижны и способны лишь к ограниченному локальному движению. Более мелкие тельца, такие как тельца Кахаля и PML-тельца, имеющие размер от 500 нм до 1 мкм, интенсивно перемещаются по ядру и претерпевают частые слияния и разделения.
Несмотря на общую структурную стабильность, ядерные тельца характеризуются значительной внутренней динамичностью. Основным компонентом ядерных телец являются особые белки, которые присутствуют и в нуклеоплазме, хотя в существенно меньшей концентрации. Эксперименты по фотообесцвечиванию показали, что ядерные тельца интенсивно обмениваются с нуклеоплазмой своими основными компонентами. В течение нескольких минут молекулярный состав ядерных телец полностью обменивается на прежде нуклеоплазматические молекулы.
Из-за отсутствия окружающих мембран форма и размер ядерных телец определяются суммой взаимодействий молекул, входящих в их состав. Среди таких взаимодействий не выявлено ковалентных, поэтому молекулы внутри телец взаимодействуют друг с другом посредством нековалентных слабых связей. Ключевым определяющим фактором является баланс приходящих и уходящих молекул: при увеличении потока приходящих молекул размер тельца увеличивается, а его снижение или увеличение потока уходящих молекул приводят к уменьшению тельца. Молекулярные механизмы, определяющие такой баланс, плохо изучены, однако в их число входят посттрансляционные модификации белков, входящих в состав ядерных телец. Контроль количества ядерных телец также плохо понятен. Даже количество ядрышек, которые формируются только вокруг фиксированного числа участков хромосом — ядрышковых организаторов, варьирует между разными тканями и типами клеток. Известно, что количество телец Кахаля регулируется маркерным белком коилином: если несколько ключевых сайтов фосфорилирования этого белка мутируют, количество телец Кахаля сокращается. Более того, размер и количество ядерных телец зависят от физиологических условий. Так, число ядрышек увеличено в активно пролиферирующих клетках. В лимфоцитах, которые активно синтезируют белки и потому нуждаются в больших количествах рРНК, ядрышки увеличиваются в размерах. Количество PML-телец положительно связано со стрессовыми условиями.
Крупные ядерные тельца, как правило, в значительной степени неподвижны, хотя и способны к небольшим перемещениям и слиянию друг с другом. Как показали эксперименты с экспериментально индуцированными интерфазными проядрышками, ведущую роль в ограничении подвижности ядерных телец играет гетерохроматин. Движение проядрышек было независимо от актина, а их слияния происходили при случайных столкновениях. При этом каждое тельце занимало отдельный компартмент, ограниченный гетерохроматином. Искусственная сверхконденсация хроматина привела к значительному снижению частоты слияния телец и, следовательно, ограничила их подвижность. Подвижность ядерных телец имеет и функциональное значение, оказывая влияние на различные аспекты функционирования генома.
Формирование
По способу формирования ядерные тельца можно разделить на два класса: зависящие от активности и не зависящие от активности. К первому классу относятся тельца, которые формируются в местах протекания определённых ядерных процессов, таких как транскрипция, и их морфология строго зависит от интенсивности процесса. К числу таких телец относится ядрышко, которое формируется на транскрибирующихся кластерах генов рРНК (ядрышковых организаторах). При подавлении транскрипции рДНК ядрышко подвергается быстрой структурной реорганизации, а доставка в ядро дополнительных генов рРНК на плазмидах приводит к появлению дополнительных ядрышек. Тельца гистоновых локусов формируются вокруг генов гистонов при активации транскрипции этих генов в начале репликации ДНК в ходе S-фазы. К этому же классу относятся стрессовые ядерные тельца и ядерные спеклы. Ко второму классу относят тельца, для формирования которых нет нужды в каком-то ядерном процессе. Такие ядерные тельца образуются в нуклеоплазме и впоследствии могут ассоциироваться с каким-то конкретным местом в ядре. Таковы тельца Кахаля и PML-тельца. Иногда они располагаются в определённых местах ядра и даже связаны со специфическими локусами, однако формируются в нуклеоплазме и приобретают такую связь позже. Например, при активации генов малых ядерных РНК U2 они подвергаются направленному, актин-зависимому перемещению к ранее сформированным тельцам Кахаля.
Формирование ядерного тельца начинается с события нуклеации. В ходе нуклеации ключевые компоненты тельца утрачивают подвижность, группируются вместе и привлекают другие «строительные блоки». У телец, зависящих от активности, нуклеацию запускают процессы, необходимые для формирования телец. В случае ядрышка нуклеация происходит при накоплении ядрышковых белков на рДНК и пре-рРНК, а в случае телец гистоновых локусов — при скоплении факторов процессинга 3'-конца гистоновых пре-мРНК. У телец, не зависящих от активности, нуклеаторами, вероятно, служат структурные белки или РНК, однако к настоящему моменту подобные нуклеаторы не были идентифицированы.
Некоторые ядерные тельца могут формироваться de novo (с нуля) в физиологических или экспериментальных условиях. Например, возможно формирование ядрышек de novo при введении в клетки минигенов рРНК в составе плазмид. Подобное явление описано для оогенеза у лягушки Xenopus, в ооцитах которой при этом процессе происходят амплификация тысяч внехромосомных генов рРНК и попутное формирование множества маленьких ядрышек. Ядерные спеклы тоже могут формироваться de novo при активации процессов транскрипции в клетке после глобального подавления. При вирусных инфекциях происходит быстрое формирование PML-телец: ключевые белки PML-телец окружают вирусный геном с образованием полноценного тельца. Эта реакция, по-видимому, служит реакцией врождённого иммунитета, направленной против вирусов. Однако наиболее отчётливо формирование de novo показано для телец Кахаля. Если в клетках, в норме не имеющих телец Кахаля, временно вызвать сверхэкспрессию компонентов этих телец, то тельца Кахаля действительно будут формироваться. Кроме того, если искусственно иммобилизировать на хроматине в случайных локусах компоненты телец Кахаля, то они будут формироваться в этих местах.
В состав многих ядерных телец входят молекулы РНК, которые нередко играют важную роль в сборке этих телец. РНК может участвовать в биогенезе ядерных телец двумя способами. Во-первых, РНК могут служить шаблонами для сборки телец, например, в случае большинства телец, зависящих от активности, которые формируются вокруг сайтов с активной транскрипцией. Такие РНК привлекают входящие в состав ядерных телец РНК-связывающие белки, запуская формирование телец. Во-вторых, РНК может выступать архитектурным элементом в ядерных тельцах. Например, для формирования параспеклов необходима NEAT1 (также известная как MEN-ε/β) — длинная стабильная полиаденилированная молекула РНК, локализованная в ядре. Нокдаун этой РНК при помощи РНК-интерференции приводит к разрушению параспеклов. Кроме того, параспеклы не выявляются в ядрах человеческих эмбриональных стволовых клеток, которые не экспрессируют NEAT1.
Теоретически возможны два основных механизма сборки ядерных телец:
- сборка может включать ряд последовательных жёстко контролируемых шагов;
- сборка может происходить в результате случайных взаимодействий компонентов ядерных телец без чёткого порядка.
Описанный выше эксперимент по сборке телец Кахаля в местах иммобилизации на хроматине ключевых компонентов этих телец свидетельствует в пользу последнего пути. Однако вопрос о том, что происходит при сборке телец, зависящих от активности, остаётся открытым.
В основе формирования ядерных телец могут лежать не только взаимодействия белок-белок и белок-РНК, но и жидкостно-жидкостные фазовые переходы (англ. Liquid–liquid phase transitions, LLPS), которые обеспечиваются способствующими агрегации доменами белков ядерных телец. С помощью модели фазовых переходов можно объяснить жидкостно-подобные свойства ядерных телец, такие как способность к слиянию и разделению, а также их быструю внутриядерную динамику. Возможно, что и гетерохроматин сам по себе обладает свойствами капель жидкости. Экспериментально показано, что белки hnRNPA1 и FUS, входящие в состав цитоплазматических стрессовых гранул и параспеклов, могут обеспечивать жидкостно-жидкостное разделение фаз (англ. liquid–liquid phase separation, LLPS) в присутствии РНК. Показано, что некоторые белковые домены подвергаются LLPS, только когда комбинируются в особых концентрациях. В каждом ядерном тельце может быть своё соотношение белков, обеспечивающих LLPS. LLPS подвергаются белковые домены, связанные с агрегацией, такие как прионоподобные домены, а также домены, способствующие полимеризации (например, биспиральный домен (англ. coiled-coil)), и участки с невыраженной структурой (англ. low complexity regions). Разнообразные ядерные структуры, образовавшиеся за счёт разделения фаз, задействованы на различных этапах экспрессии генов, таких как транскрипция и процессинг РНК, оказывают влияние на эпигенетический статус генов и играют роль в развитии многих заболеваний. В формировании ядерных телец за счёт разделения фаз могут принимать участие фосфоинозитиды. В 2018 году в ядрах клеток самых разных организмов были обнаружены тельца, содержащие фосфатидилинозитол-4,5-бисфосфат; они известны как ядерные липидные островки (англ. Nuclear Lipid Islets, NLIs). Вероятно, ядерные липидные островки играют важную роль в регуляции экспрессии генов, выступая в качестве платформ для связывания различных белков и облегчая формирование транскрипционных фабрик.
Ядерные тельца и митоз
Сборка и разборка ядерных телец играют важную роль в их наследовании дочерними клетками при делении. Некоторые ядерные тельца, которые присутствуют в клетках в большом количестве копий, при митозе не разбираются, а разделяются примерно поровну между дочерними клетками за счёт их случайного распределения по объёму клетки. Другие ядерные тельца, напротив, разбираются при клеточном делении и снова собираются при вступлении дочерних клеток в G1-фазу.
Так, ядрышко при митозе разбирается, поскольку транскрипция рРНК приостанавливается из-за фосфорилирования транскрипционных факторов РНК-полимеразы I, а также факторов процессинга рРНК. В начале профазы на периферии конденсированных хромосом накапливаются непроцессированные или частично процессированные пре-рРНК вместе со многими факторами процессинга. После разрушения ядерной оболочки они выходят в цитоплазму и в анафазе формируют множество очень подвижных мелких телец. В начале телофазы, когда происходит восстановление транскрипции генов рРНК, эти мелкие тельца разбираются, и далее пре-рРНК и факторы процессинга образуют проядрышковые тельца (англ. prenucleolar bodies) в нуклеоплазме только что сформированных ядер дочерних клеток. В конце телофазы хромосомы деконденсируются, и пре-рРНК и факторы процессинга выходят из проядрышковых телец, формируя ядрышко вокруг ядрышковых организаторов. Для формирования ядрышка после митоза также необходимы активность РНК-полимеразы I и возобновление процессинга пре-рРНК.
В начале митоза ядерные спеклы разбираются, а их компоненты распределяются беспорядочно по цитоплазме. Сборка спеклов начинается в телофазе. Параспеклы остаются стабильными на протяжении всего клеточного цикла вплоть до анафазы, когда они становятся беспорядочно разбросанными по клетке (цитоплазматические параспеклы). Цитоплазматические параспеклы исчезают в начале телофазы, а формирование ядерных параспеклов начинается по завершении клеточного деления. Тельца гистоновых локусов существуют до ранней прометафазы и окончательно разбираются в метафазе, а заново образуются в телофазе. Тельца Кахаля в начале митоза не разбираются, а выходят в цитоплазму, где не находятся в физическом контакте с конденсированными хромосомами. Количество и размер телец Кахаля почти не меняются от метафазы до телофазы. Когда в телофазе формируется ядерная оболочка, цитоплазматические тельца Кахаля разбираются, а их ключевой компонент — белок коилин — быстро заходит в ядро, где поначалу локализуется беспорядочно, но к G1-фазе в дочерних клетках формируются нормальные ядерные тельца Кахаля. Количество PML-телец в начале митоза уменьшается, поскольку их главный компонент — белок PML — образует характерные митотические скопления, утрачивая связь с другими белками PML-телец. Образование в ядре PML-телец начинается в G1-фазе, однако даже в течение G1-фазы в цитоплазме всё ещё обнаруживаются большие скопления белка PML, которые далее медленно сокращаются.
Разнообразие
В таблице ниже перечислены ключевые ядерные тельца, их свойства и выполняемые функции.
| Ядерное тельце | Функции | Характерные компоненты | Типичный размер (в мкм) | Количество на ядро |
|---|---|---|---|---|
| Ядрышко | Биогенез рибосом | Машинерия РНК-полимеразы I, факторы процессинга рРНК и сборки рибосомных субъединиц | 3—8 | 1—4 |
| Спеклы | Накопление и сборка факторов сплайсинга | Факторы сплайсинга пре-мРНК | 2—3 | 20—50 |
| Стрессовые ядерные тельца | Регуляция транскрипции и сплайсинга в условиях стресса | HSF1, HAP | 1—2 | 3—6 |
| Тельце гистоновых локусов | Процессинг пре-мРНК гистонов | NPAT, FLASH, U7 мяРНП | 0,2—1,2 | 2—4 |
| Тельце Кахаля | Биогенез, созревание и кругооборот малых РНК | Коилин, SMN | 0,2—1,5 | 1—10 |
| PML-тельце | Регуляция стабильности генома, репарация ДНК, контроль транскрипции, защита от вирусов | PML | 0,1—1 | 10—30 |
| Параспеклы | Регуляция мРНК, редактирование РНК | Некодирующие РНК NEAT1/MENε/β, белки PSP1, p54nrb/NONO | 0,2—1 | 2—20 |
| Околоядрышковый компартмент | Посттранскрипционная регуляция набора РНК, синтезированных РНК-полимеразой III | PTB | 0,2—1 | 1—2 |
Ядрышко

Ядрышко — это отдельная плотная структура в ядре. Она не окружена мембраной и формируется в области расположения рДНК — тандемных повторов генов рибосомной РНК (рРНК), называемых ядрышковыми организаторами. Главные функции ядрышка — синтез рРНК и образование рибосом. Структурная целостность ядрышка зависит от его активности, и инактивация генов рРНК приводит к смешению ядрышковых структур.
На первой стадии образования рибосом фермент РНК-полимераза I транскрибирует рДНК и образует пре-рРНК, которая далее разрезается на 5,8S, 18S и 28S рРНК. Транскрипция и посттранскрипционный процессинг рРНК происходят в ядрышке при участии малых ядрышковых РНК (мякРНК), некоторые из которых происходят из сплайсированных интронов мРНК генов, кодирующих белки, связанные с работой рибосом. Собранные рибосомные субъединицы — это самые крупные структуры, проходящие через ядерные поры.
При рассматривании под электронным микроскопом в ядрышке можно выделить три компонента: фибриллярные центры (ФЦ), окружающий их плотный фибриллярный компонент (ПФК) и гранулярный компонент (ГК), который, в свою очередь, окружает ПФК. Транскрипция рРНК происходит в ФЦ и на границе ФЦ и ПФК, поэтому при активации образования рибосом ФЦ становятся хорошо различимы. Разрезание и модификации рРНК происходят в ПФК, а последующие этапы образования рибосомных субъединиц, включающие загрузку рибосомных белков, происходят в ГК.
Тельце Кахаля
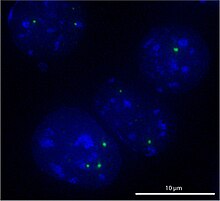
Тельце Кахаля (ТК) — ядерное тельце, имеющееся у всех эукариот. Оно идентифицируется по наличию сигнатурного белка коилина и специфических РНК (scaРНК). В ТК также содержится белок SMN (англ. survival of motor neurons). В ТК наблюдается высокая концентрация сплайсирующих малых ядерных рибонуклеопротеинов (мяРНП) и других факторов процессинга РНК, поэтому считается, что ТК служат местами сборки и/или посттранскрипционной модификации факторов сплайсинга. ТК присутствует в ядре во время интерфазы, но исчезает в митозе. В биогенезе ТК прослеживаются свойства самоорганизующейся структуры.
Когда внутриклеточная локализация SMN впервые изучалась методом иммунофлуоресценции, то белок обнаруживался во всей цитоплазме, а также в ядрышковом тельце, сходном по размеру с ТК и часто расположенном рядом с ним. По этой причине данное тельце было названо «близнецом ТК» (англ. gemini of CB) или просто gem. Однако оказалось, что линия клеток HeLa, в которой было открыто новое тельце, была необычной: в других линиях клеток человека, а также у плодовой мушки Drosophila melanogaster SMN колокализовался с коилином в ТК. Поэтому в общем случае SMN можно рассматривать как важный компонент ТК, а не как маркер отдельного ядерного тельца.
Тельце гистоновых локусов
Тельце гистоновых локусов (англ. histone locus body, HLB) содержит факторы, необходимые для процессинга пре-мРНК гистонов. Как и следует из названия, тельца гистоновых локусов ассоциированы с генами, кодирующими гистоны; поэтому предполагается, что в тельцах гистоновых локусов концентрируются факторы сплайсинга. Тельце гистоновых локусов присутствует в клетке во время интерфазы и исчезает с наступлением митоза. Тельце гистоновых локусов нередко рассматривается вместе с тельцем Кахаля по нескольким причинам. Во-первых, в некоторых тельцах гистоновых локусов содержится маркер телец Кахаля — коилин. Во-вторых, эти тельца нередко физически находятся рядом, поэтому между ними наблюдается некоторое взаимодействие. Наконец, очень крупные тельца Кахаля ооцитов земноводных обладают свойствами обоих телец.
PML-тельца
Тельца промиелоцитной лейкемии (англ. Promyelocytic leukaemia bodies), или PML-тельца, — сферические тельца, разбросанные по всей нуклеоплазме и достигающие около 0,1—1,0 мкм в диаметре. Они известны также под такими названиями, как ядерный домен 10 (англ. nuclear domain 10 (ND10)), тельца Кремера (англ. Kremer bodies) и онкогенные домены PML (англ. PML oncogenic domains). Тельца PML названы по одному из своих ключевых компонентов — белку промиелоцитной лейкемии (PML). Они часто наблюдаются ассоциированными с тельцами Кахаля и тельцами деления (англ. cleavage body). PML-тельца принадлежат ядерному матриксу и могут быть задействованы в таких процессах, как репликация ДНК, транскрипция и эпигенетический сайленсинг генов. Ключевым фактором организации этих телец выступает белок PML, который привлекает другие белки; последние, по представлениям XXI века, объединены лишь тем, что они SUMOилированы. Мыши, у которых ген PML делетирован, лишены PML-телец, однако развиваются и живут нормально — это означает, что PML-тельца не выполняют незаменимых биологических функций.
Спеклы
Спеклы (англ. speckle) — это ядерные тельца, которые содержат факторы сплайсинга пре-мРНК и располагаются в интерхроматиновых участках нуклеоплазмы клеток млекопитающих. При флуоресцентной микроскопии спеклы выглядят как пятнистые тельца неправильной формы, различных размеров, а при электронной микроскопии — как кластеры интерхроматиновых гранул. Спеклы — динамические структуры, и содержащиеся в них белки и РНК могут перемещаться между спеклами и другими ядерными тельцами, включая участки активной транскрипции. На основании исследований состава, структуры и поведения спеклов была создана модель, объясняющая функциональную компартментализацию ядра и организацию механизма экспрессии генов, сплайсирующих малые ядерные рибонуклеопротеины и другие белки, необходимые для сплайсинга пре-мРНК. Из-за изменяющихся потребностей клетки состав и расположение спеклов изменяются согласно транскрипции мРНК и посредством регуляции фосфорилирования специфических белков. Сплайсирующие спеклы также известны как ядерные спеклы, компартменты сплайсирующих факторов, кластеры интерхроматиновых гранул и B-снурпосомы (англ. B snurposomes). B-снурпосомы найдены в ядрах ооцитов земноводных и зародышах плодовой мушки Drosophila melanogaster. На электронных микрофотографиях B-снурпосомы предстают прикреплёнными к тельцам Кахаля или отдельно от них. Кластеры интерхроматиновых гранул служат местами скопления факторов сплайсинга.
Параспеклы
Параспеклы — это ядерные тельца неправильной формы, располагающиеся в интерхроматиновом пространстве ядра. Впервые они были описаны у клеток HeLa, у которых имеется 10—30 параспеклов на ядро, но сейчас параспеклы обнаружены во всех первичных клетках человека, в клетках трансформированных линий и на срезах тканей. Своё название они получили из-за своего расположения в ядре — вблизи спеклов.
Параспеклы — динамические структуры, которые изменяются в ответ на изменения в метаболической активности клетки. Они зависят от транскрипции, и в отсутствие транскрипции, проводимой РНК-полимеразой II, параспеклы исчезают, а все входящие в их состав белки (PSP1, p54nrb, PSP2, CFI(m)68 и PSF) формируют серповидный околоядрышковый кэп. Этот феномен наблюдается в ходе клеточного цикла: параспеклы присутствуют в интерфазе и всех фазах митоза, за исключением телофазы. В ходе телофазы формируются дочерние ядра, и РНК-полимераза II ничего не транскрибирует, поэтому белки параспеклов формируют околоядрышковый кэп. Параспеклы участвуют в регуляции экспрессии генов, накапливая те РНК, где есть двухцепочечные участки, которые подвергаются редактированию, а именно превращению аденозина в инозин. Благодаря этому механизму параспеклы задействованы в контроле экспрессии генов при дифференцировке, вирусной инфекции и стрессе.
Околоядрышковый компартмент
Околоядрышковый компартмент (ОК) — ядерное тельце неправильной формы, которое характеризуется тем, что располагается на периферии ядрышка. Несмотря на физическую связь, эти два компартмента структурно различны. Обычно ОК обнаруживают в клетках злокачественных опухолей. ОК — динамическая структура и содержит очень много РНК-связывающих белков и РНК-полимеразу III. Структурная стабильность ОК обеспечивается транскрипцией, осуществляемой РНК-полимеразой III, и наличием ключевых белков. Поскольку присутствие ОК обычно связано со злокачественностью и со способностью к метастазированию, их рассматривают как потенциальные маркеры рака и других злокачественных опухолей. Показана ассоциация ОК со специфическими локусами ДНК.
Стрессовые ядерные тельца
Стрессовые ядерные тельца формируются в ядре при тепловом шоке. Они образуются при непосредственном взаимодействии транскрипционного фактора теплового шока 1 (HSF1) и перицентрических тандемных повторов в последовательности сателлита III, что соответствует сайтам активной транскрипции некодирующих транскриптов сателлита III. Распространено мнение, что такие тельца соответствуют очень плотно упакованным формам рибонуклеопротеиновых комплексов. Считается, что в клетках, подвергающихся стрессу, они участвуют в быстрых, временных и глобальных изменениях в экспрессии генов посредством различных механизмов — например, ремоделирования хроматина и захватывания факторов транскрипции и сплайсинга. В клетках, находящихся в нормальных (не стрессовых) условиях, стрессовые ядерные тельца обнаруживаются редко, однако их количество резко увеличивается под действием теплового шока. Стрессовые ядерные тельца найдены только в клетках человека и других приматов.
Ядерные тельца-сироты
Ядерные тельца-сироты (англ. orphan nuclear bodies) — нехроматиновые ядерные компартменты, которые исследованы гораздо хуже, чем другие, хорошо охарактеризованные, структуры ядра. Некоторые из них выступают как места, в которых белки модифицируются белками SUMO и/или происходит протеасомная деградация белков, помеченных убиквитином. Ниже в таблице приведены характеристики известных ядерных телец-сирот.
| Ядерное тельце | Описание | Типичный размер (в мкм) | Количество на ядро |
|---|---|---|---|
| Кластосома | Концентрирует протеасомные комплексы 20S и 19S и белки, связанные с убиквитином. Обнаруживается главным образом тогда, когда стимулируется активность протеасом, и разбирается при ингибировании активности протеасом. | 0,2—1,2 | 0—3 |
| Тельце деления (англ. cleavage body) | Обогащено факторами деления CstF и CPSF, а также белком DDX1, содержащим DEAD-бокс. Обнаруживается в основном в S-фазе, ингибирование транскрипции на него не влияет. | 0,2—1,0 | 1—4 |
| Домен OPT | Обогащён факторами транскрипции Oct1 и PTF. Частично колокализуется с сайтами транскрипции. Обнаруживается в основном в поздней G1-фазе, разбирается при ингибировании транскрипции. | 1,0—1,5 | 1—3 |
| Тельце Polycomb | Обнаруживается в клетках человека и дрозофилы, обогащено белком PcG. У человека накапливает белки RING1, BMI1, HPC, может быть связано с околоцентромерным гетерохроматином. | 0,3—1,0 | 12—16 |
| Тельце Sam68 | Накапливает белок Sam68 и схожие с ним белки SLM-1 и SLM-2. Разбирается при ингибировании транскрипции. Вероятно, обогащено РНК. | 0,6—1,0 | 2—5 |
| Тельце SUMO | Обогащено белками SUMO и SUMO-конъюгирующим ферментом Ubc9. Концентрирует транскрипционные факторы pCREB, CBP, c-Jun. | 1—3 | 1—3 |
Литература
- The Nucleus / Tom Misteli, David L. Spector. — New York: Cold Spring Harbor Perpectives in Biology, 2011. — 463 p. — ISBN 978-0-87969-894-2.
